CPCC が提供する臨床試験

試験全体をトータルサポート
CPCCでは、試験の立案、試験計画書作成、被験者募集‧管理、クリニックでの検査、専門医師のサポート、データ処理‧統計解析、報告書作成‧論文投稿まで、一貫してサポートいたします。
トクホや機能性表示食品取得を目的とした参加者人数100名以上の規模の大きい臨床試験から、商品の効果を探索する10名前後のパイロット試験まで幅広く対応することができます。
提携クリニック、医療機関や大学と協力し、原料やサプリメント、健康食品、化粧品などのより高い安全性の確保や訴求力の底上げをサポートいたします。
臨床試験例

clinicaltrials 01
有効性試験
原料や製品の有効性を評価・確認します。
製品の有効性を統計学的に評価することができます。
試験実例
-
免疫試験
-
ストレス試験
-
自律神経試験
-
認知機能試験
-
口腔機能試験
-
運動時脂質代謝試験
-
安静時代謝試験
-
血流試験
-
血管内皮試験
-
血圧試験
-
腸内環境試験
-
睡眠試験
-
運動機能試験
-
血糖値試験
-
中性脂肪試験
-
内臓脂肪試験
-
肌試験

clinicaltrials 02
安全性試験
原料や製品がヒトに与える影響を検証します。
製品の安全性に対する科学的根拠を得ることができ、消費者に対して製品が安全であることを統計学的に評価することができます。
試験実例
-
過剰摂取安全性試験
-
長期摂取安全性試験

clinicaltrials 03
機能性表示・トクホ試験
特定保健用食品(トクホ)とは、有効性や安全性について国の審査を受け、許可を得なければなりません。そのためには、主に最終製品を用いて、定められた手順に沿ったヒト試験を実施して科学的根拠を示すことが必要です。
一方、機能性表示食品は、安全性及び機能性の根拠に関する情報などを、消費者庁に届け出の上、事業者の責任で表示することができます。トクホよりも広い範囲の機能性を表示することができ、生鮮食品や農産物を含めてほぼ全ての食品が対象となります。科学的根拠は、臨床試験または研究レビュー(システマティックレビュー)によって説明することが求められます。試験の方法は、トクホ試験に準じています。
CPCCではこれらの基準に沿った試験が実施可能です。
試験実例
-
用量設定試験
-
過剰摂取安全性確認試験
-
長期摂取安全性確認試験
-
有効性確認試験

clinicaltrials 04
パイロット試験
例数の多い、高コストな大規模試験を実施する前には、その実現可能性を評価する小規模試験を行うことは不可欠です。CPCCでは単回摂取試験をはじめとして、各種パイロット試験デザインを提案いたします。
試験実例
-
便通パイロット
-
肌パイロット
-
唾液分泌促進パイロット

clinicaltrials 05
使用感調査
CPCCでは、ご指定のアプリやデバイスなどを使用し、来院検査の伴わない使用感調査が可能です。
消費者に自社の商品を一定期間使用してもらうことで、日常生活の中でのデータを得ることができ、商品に対する消費者の反応や改善点を知ることができます。
試験実例
-
試験品嗜好性調査
-
デバイス使用感調査
免疫試験
試験概要
| 研究目的 | 試験食品摂取による免疫賦活効果確認 |
|---|---|
| 説明 | ヘルスクレームとして「免疫」での機能性食品届出のニーズにも対応しうるように、関連専門機関とも連携を取り、それぞれの試験食品の有用性評価や作用機序解明の目的に合った免疫マーカー、試験デザインなどを提案しております。 |
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 4回:スクリーニング、0W、6W、12W |
| 症例数 | 100名(1群50名×2群) |
| 対象 | BMI:30未満 |
| 評価項目 | 【フローサイトメトリーによる免疫細胞解析】 pDC検査、mDC検査、T細胞、B細胞 【細胞アッセイ】 NK細胞活性、好中球殺菌能、好中球貪食能 【血液・唾液検査】 サイトカイン類(インターロイキン6、インターロイキン8、インターロイキン12など) |
アウトライン
ストレス試験
試験概要
| 研究目的 | 試験食品摂取によるストレス低減効果確認 |
|---|---|
| 説明 | ストレスは外部からのさまざまな刺激によって自分の心や体に過剰な負荷が生じることです。急性的なストレス、持続的なストレスは、どちらも身体へ様々な不調を引き起こす原因になります。 |
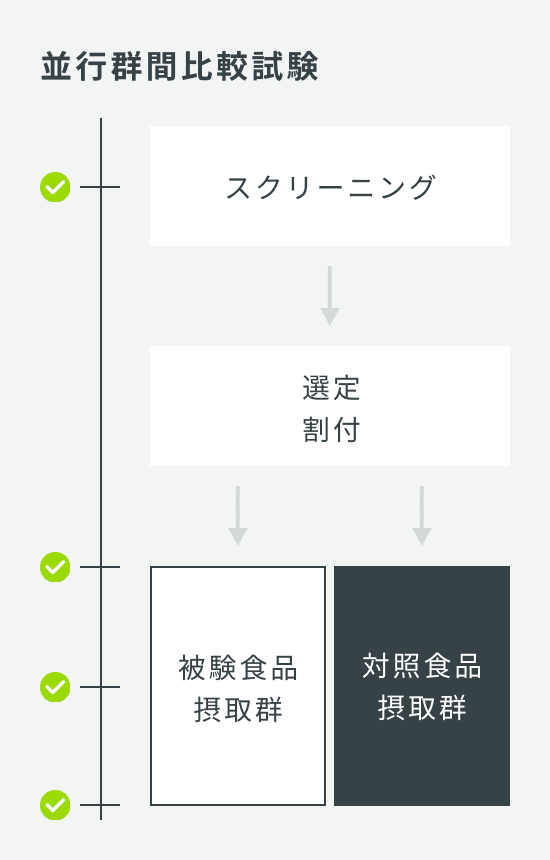
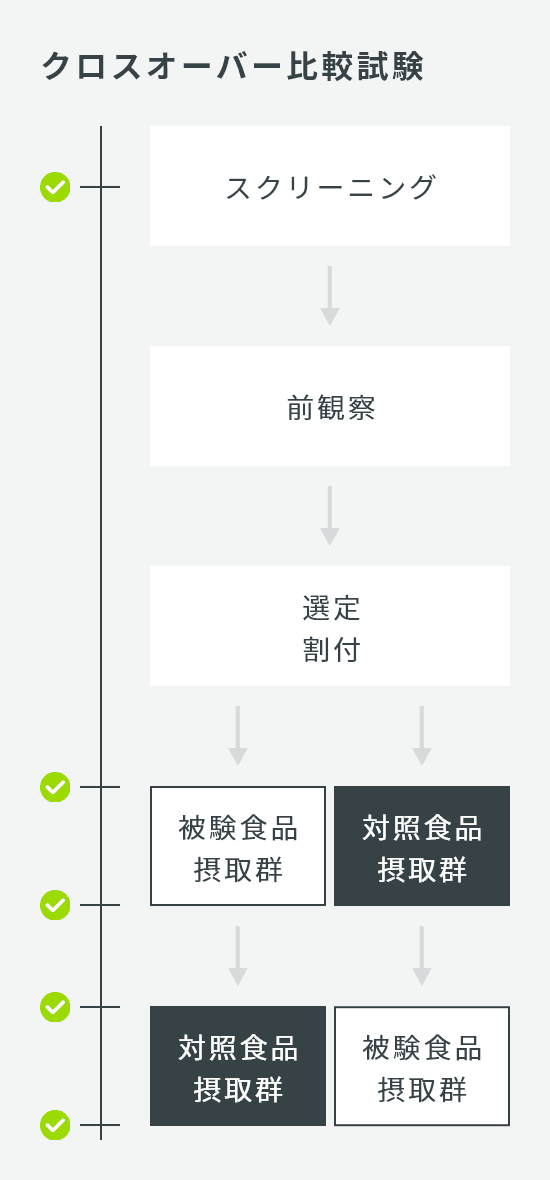
| 試験デザイン | クロスオーバー比較試験または並行群間比較試験 |
| 介入期間 | 単回摂取または12週間 |
| 検査回数 | クロスオーバー比較試験 3回:スクリーニング、第1期検査、第2期検査 並行群間比較試験 4回:スクリーニング、0W、6W、12W |
| 症例数 | クロスオーバー比較試験 30名 並行群間比較試験 60名(1群30名×2群) |
| 対象 | ストレスを感じている者 |
| 評価項目 | 【クロスオーバー比較試験】 主観アンケート、唾液中コルチゾール、唾液中アミラーゼ、唾液中クロモグラニンA 【並行群間比較試験】 主観アンケート 【クロスオーバー比較試験・並行群間試験共通】 血液抗酸化力検査(d-ROM、BAP)、尿中8-OHdG |
アウトライン

自律神経試験
試験概要
| 研究目的 | 試験食品摂取による自律神経作用確認 |
|---|---|
| 説明 | 仕事や家庭でのストレス、加齢(特に女性)、季節や天候の変化などの負荷が、長く続いたり急激に襲い掛かると、自律神経が過度に緊張した状態となってしまい、身体に様々な問題が出てきます。 |
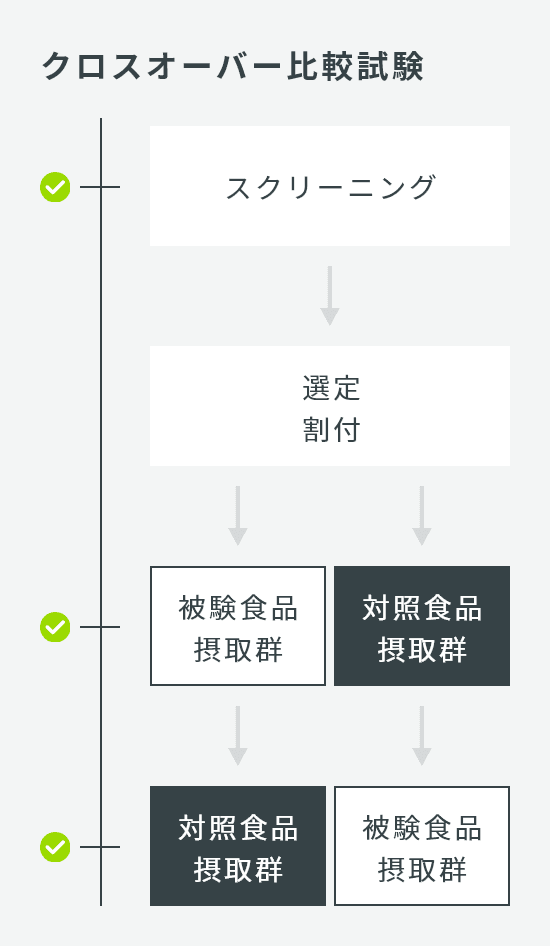
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回摂取 |
| 検査回数 | 3回:スクリーニング、第1期検査、第2期検査 |
| 症例数 | 30名 |
| 対象 | ストレスを感じている者 |
| 評価項目 | 【機器測定】 瞳孔対光反射、皮膚温測定、フリッカ測定、脳実行機能測定、脳ストレス測定 【アンケート】 主観アンケート 【唾液検査】 唾液中オキシトシン、唾液中コルチゾール、唾液中クロモグラニンA |
アウトライン
認知機能試験
試験概要
| 研究目的 | 試験食品摂取による認知機能改善効果確認 |
|---|---|
| 説明 | 高齢者における認知症など脳機能障害の患者数は今後ますます増加傾向となることが予想されます。 認知症の予防、および初期症状の改善を目的に、食品を通して介入することは、重篤な脳機能障害への進展を未然に防止することに繋がり、健康の維持・増進に役立ちます。 |
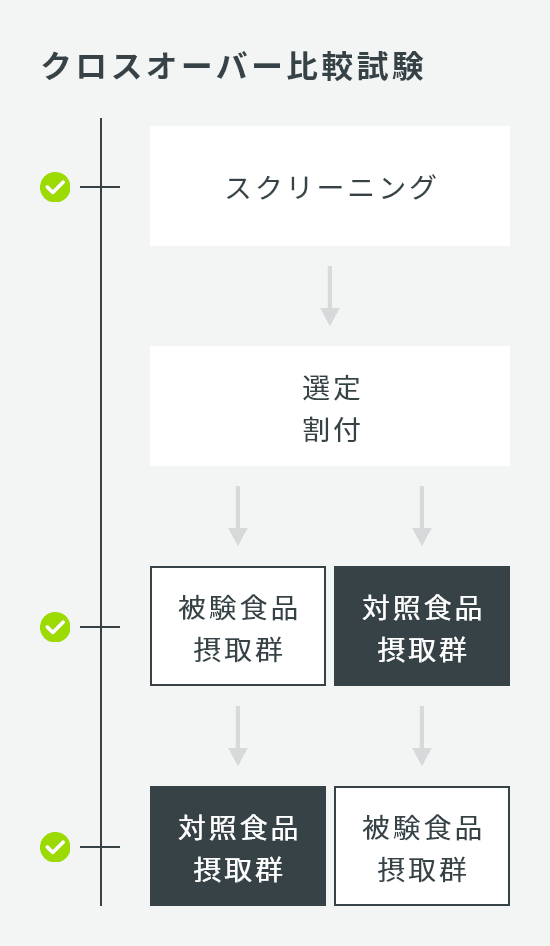
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 4回:スクリーニング、0W、6W、12W |
| 症例数 | 100名(1群50名×2群) |
| 対象 | 物忘れの自覚がある高齢者 |
| 評価項目 | 【認知機能評価テスト】 コグニトラックスによる認知機能検査、MMSE-J(Mini-Mental State Examination)、TMT(Trail Making Test)、MoCA-J(Montoreal Cognitive Assessment) 【アンケート】 QOLアンケート 【血液検査】 血中アミロイドβ測定、血中BDNF測定 |
アウトライン

口腔機能試験
試験概要
| 研究目的 | 試験食品摂取による口腔機能改善効果確認 |
|---|---|
| 説明 | 日本における歯周病の有病状況は、他の疾患に類を見ないほど高率を示しており、歯周病や口臭を改善する機能性食品の発売も期待されています。 弊社では歯科クリニックとの連携により、口腔検査の実施が可能です。 |
| 試験デザイン | 連続:並行群間比較試験 単回:クロスオーバー比較試験 |
| 介入期間 | 1週間-12週間 |
| 検査回数 | 連続:スクリーニング、0W、4W、8W、12W 単回:スクリーニング、第1期検査、第2期検査 |
| 症例数 | 連続:並行群間比較試験 60名(1群30名×2群) 単回:30名 |
| 対象 | 健常者 |
| 評価項目 | 【唾液分泌検査】 刺激時唾液量測定(サクソン法)、安静時唾液量測定(吐唾法) 【口臭・咬合検査】 口臭測定(オーラルクロマ)、咬合力検査(オクルーザルフォースメーター) 【唾液検査】 唾液中コルチゾール、クロモグラニン、アミラーゼ、IgA 【口腔細菌検査】 舌表面細菌:10菌種:MRSA、MSSA、緑膿菌、β溶連菌、肺炎球菌、インフルエンザ菌、肺炎桿菌、セラチア菌、カタル球菌、歯周病関連菌:6菌種:Aa菌、Pg菌、Pi菌、Tf菌、Td菌、Fn菌、齲蝕関連菌:総レンサ球菌、ミュータンスレンサ球菌、乳酸桿菌、次世代シーケンサーでの口腔菌叢の網羅的解析 |
アウトライン
運動時脂質代謝試験
試験概要
| 研究目的 | 試験食品摂取による運動時代謝改善効果確認 |
|---|---|
| 説明 | 運動時の代謝の促進を非侵襲的に確認するには、軽運動負荷を与えた時の呼気ガス測定による呼吸商や脂肪酸化量の変動を活用する方法が一般的に用いられています。 |
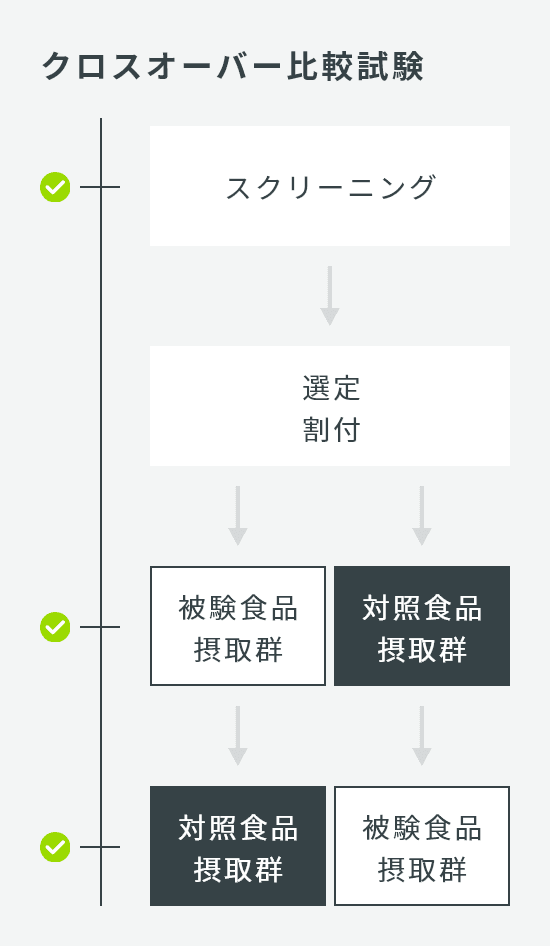
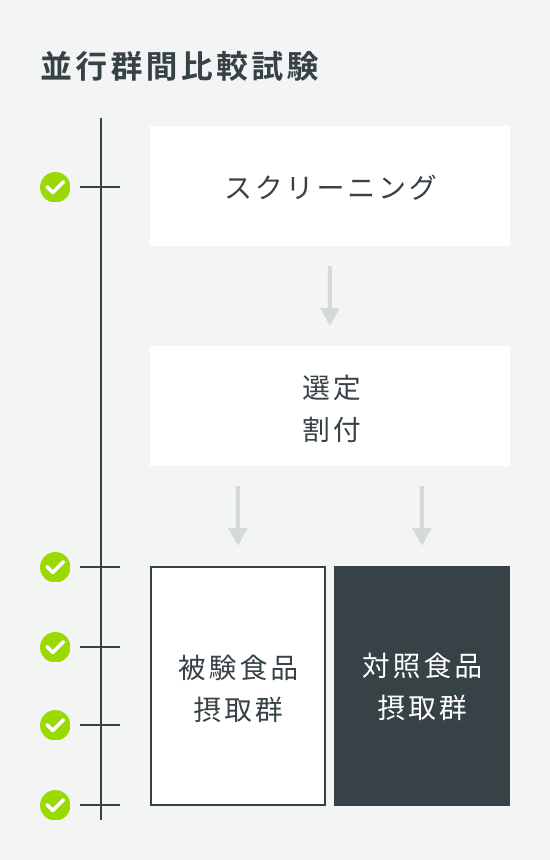
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回 |
| 検査回数 | スクリーニング、第1期検査、第2期検査 |
| 症例数 | 30名 |
| 対象 | 健常者 |
| 評価項目 | エアロバイク➀にて30分間運動時のエアロモニターでの呼吸商測定 (➀:ご希望の強度、時間で運動負荷が可能です。検査機器ページ) エアロモニター②での呼吸商測定(②:運動中の呼気、吸気の流量、酸素濃度、二酸化炭素濃度を測定することにより、運動中の代謝循環を測定します。検査機器ページ) |
アウトライン

安静時代謝試験
試験概要
| 研究目的 | 試験食品摂取による安静時代謝改善効果確認 |
|---|---|
| 説明 | 老化の進行にともない基礎代謝は低下し、肥満症を誘導しやすくなります。 ただ単に太りやすくなるということのみでなく、肌荒れ・むくみ・疲れ・冷え症・生理不順の原因にもなり、加齢による身体活動量の低下や、筋肉量減少による基礎代謝量の低下など複数の要因が影響していると考えられます。このような背景の下、基礎代謝の維持・向上への解決策として、安静時のエネルギー消費量を増加させる食品の開発が期待されています。 |
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回 |
| 検査回数 | スクリーニング、第1期検査、第2期検査 |
| 症例数 | 30名 |
| 対象 | 健常者 |
| 評価項目 | ヒューマンカロリーメーターでの呼吸商測定 (温度・湿度・流量が一定にコントロールされた、高気密チャンバー型の間接型熱量測定装置です。) |
アウトライン
血流試験
試験概要
| 研究目的 | 試験食品摂取による血流改善効果確認 |
|---|---|
| 説明 | 血流の悪化は冷え性、肩こりなどの不定愁訴を引き起こす原因となる恐れがあり、血流を改善することはQOL改善への貢献が期待されています。 |
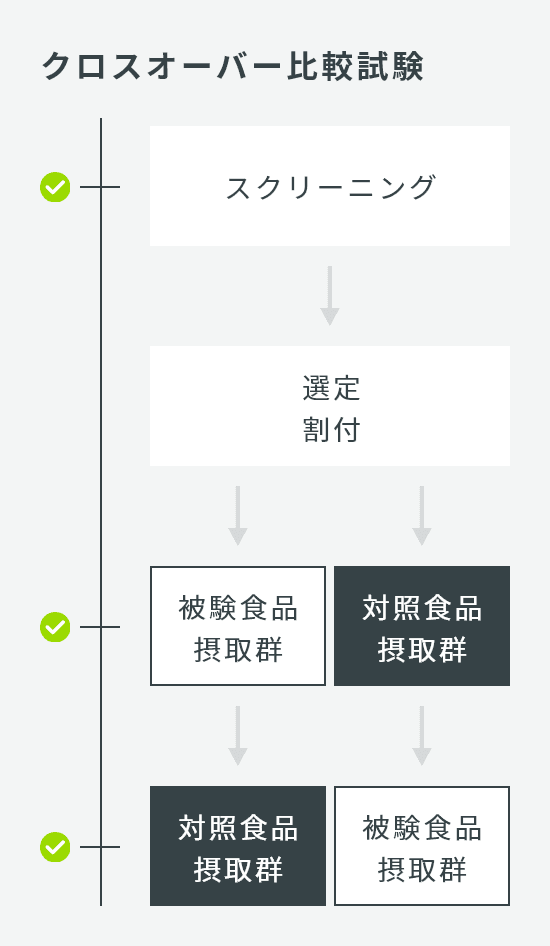
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回 |
| 検査回数 | スクリーニング、第1期検査、第2期検査 |
| 症例数 | 30名 |
| 対象 | 健常者 |
| 評価項目 | 2次元レーザー血流画像装置➀での血流評価 (➀:生体組織の血流状態を、色分布で連続的に高解像度、高速で表示します。検査機器ページ) レーザードップラー血流画像化装置②での血流量測定 (②:スキャニングによる「面」での血流分布測定と、時間を追って血流変化を計測する、従来の「一点型レーザードップラー血流計」の両方を兼ね備えています。検査機器ページ) サーモグラフィー③での表面体温測定 (③:高解像度赤外線サーモグラフィカメラで表面体温を測定します。検査機器ページ) |
アウトライン
血管内皮試験
試験概要
| 研究目的 | 試験食品摂取による血管内皮機能への影響確認 |
|---|---|
| 説明 | 近年では、生活習慣病などに起因する活性酸素傷害防御系の乱れが血管内皮機能を低下させ、動脈硬化などの血管障害を促進することが分かってきています。血管内皮機能の低下が動脈硬化などの心疾患・脳血管疾患の主要危険因子であると認識され、血管内皮機能を維持・改善することの重要性が高まってきています。 |
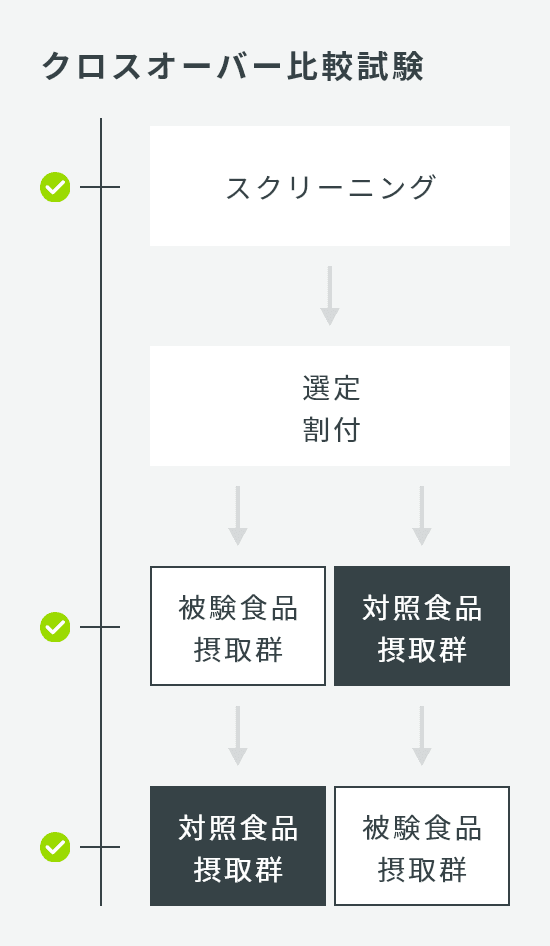
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 6回:スクリーニング1、スクリーニング2、0W、4W、8W、12W |
| 症例数 | 80名(1群40名×2群) |
| 対象 | FMD4%以上7%未満 |
| 評価項目 | FMD➀での血管内皮機能 (➀:腕を駆血した後の血流増大による上腕動脈の拡張度(%)を求める方法です。血管内皮機能が低下していると、駆血後に血管が拡張する力が弱くなることでFMD値は低下します。検査機器ページ) RH-PAT②での血管内皮機能 (②:FMD検査と同様に腕を駆血し、脈波を測定するためのプローブを指先に装着します。駆血前後の末梢動脈の血流量変化を測定します。数値はRHI(反応性充血指数)スコアで示され、血管内皮機能が低下していると値は低下します。機器ページのリンク) 血圧値 |
アウトライン
血圧試験
試験概要
| 研究目的 | 試験食品摂取による血圧値改善効果確認 |
|---|---|
| 説明 | 高血圧は脳心血管病(脳卒中および心疾患)や腎臓病の発症リスクを増大させることが知られており、特に高血圧に起因する脳心血管病は日本人の主要な死因の一つとなっています。高齢化に伴い、高血圧有病者数は今後増加する可能性があるため、機能性食品の開発が期待されています。 |
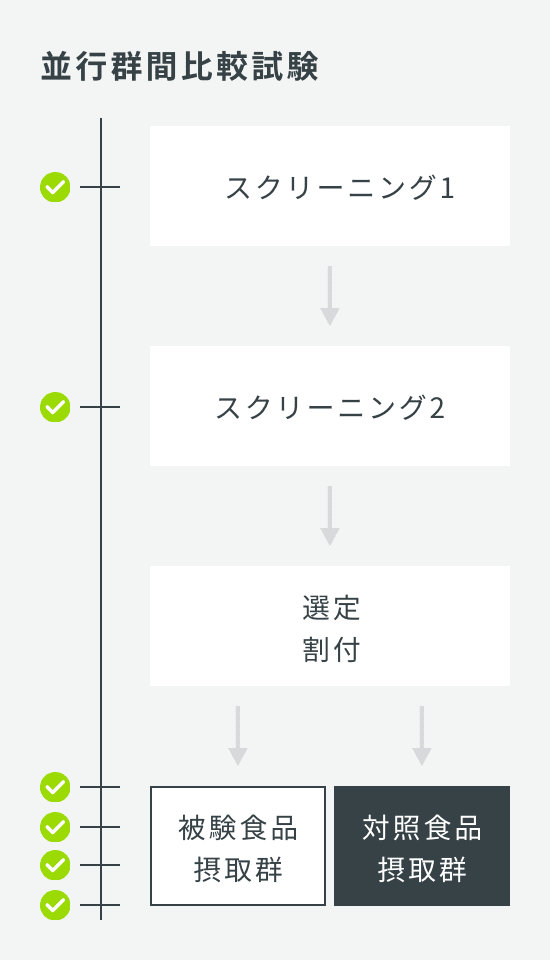
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 6回:スクリーニング1、スクリーニング2、0W、4W、8W、12W |
| 症例数 | 80名(1群40名×2群) |
| 対象 | 診療室血圧が高値血圧に該当する方 収縮期血圧130-139mmHgかつ/または拡張期血圧80-89mmHg 血圧値:高血圧治療ガイドライン2019に従い測定 |
| 評価項目 | 血圧値 |
アウトライン
腸内環境試験
試験概要
| 研究目的 | 試験食品摂取による腸内環境改善効果確認 |
|---|---|
| 説明 | 近年、腸内環境とヒトの健康や疾病との関連における研究が進展し、腸内環境の改善が生活習慣病の予防・改善に有効であることが分かっています。 腸内環境の改善は、各種疾病予防や認知症予防へ繋がり、少子超高齢化を迎えた我が国では健康長寿への重要因子と捉えることができます。 |
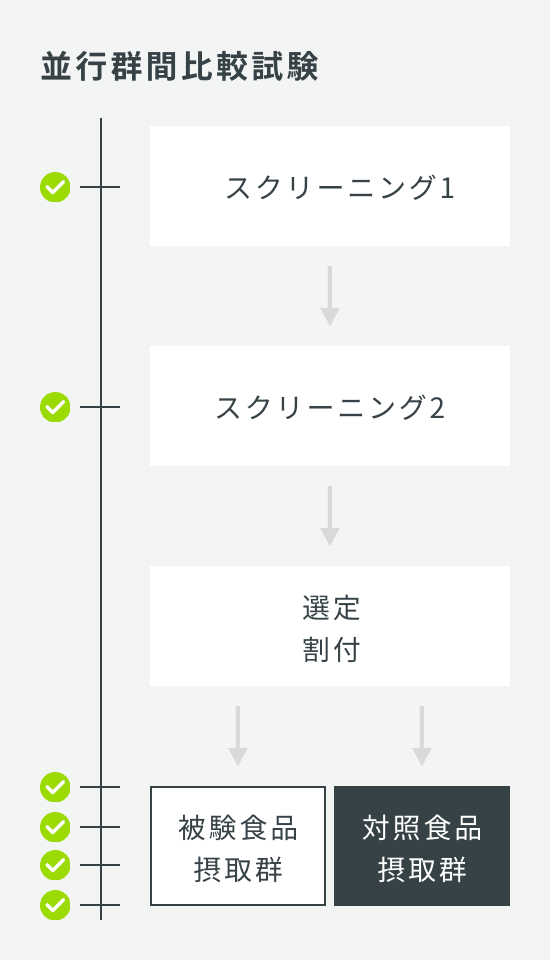
| 試験デザイン | クロスオーバー比較試験または並行群間比較試験 |
| 介入期間 | 4週間-12週間 |
| 検査回数 | クロスオーバー比較試験 5回:スクリーニング、第1期摂取開始前、第1期摂取終了時、第2期摂取開始前、第2期摂取終了時 並行群間比較試験 3回:スクリーニング、0W、4W |
| 症例数 | クロスオーバー比較試験 30名 並行群間比較試験 60名(1群30名×2群) |
| 対象 | 便秘傾向者 |
| 評価項目 | 【腸内細菌叢解析】 次世代シーケンサーでの腸内菌叢の網羅的解析、リアルタイムPCRでの腸内細菌中の特定菌の定量 【糞便中の成分分析】 有機酸、短鎖脂肪酸、腐敗産物、IgA、その他代謝物質 【糞便性状解析】 pH、水分量、アンモニア 【日誌・アンケート】 日誌での排便回数やブリストルスケール、CAS-MT |
アウトライン
睡眠試験
試験概要
| 研究目的 | 試験食品摂取による睡眠改善効果確認 |
|---|---|
| 説明 | 不眠あるいは睡眠不足は、感染症や生活習慣病といった様々な疾病への罹患リスクを増大させることが分かっており、睡眠の質を改善することは、健康寿命の延伸へ繋がります。 |
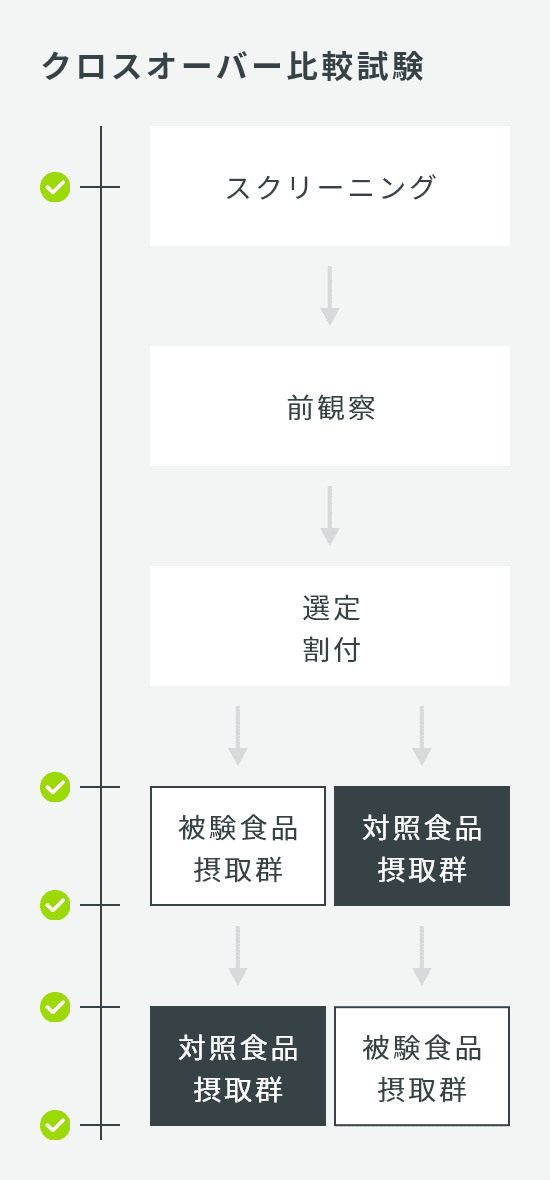
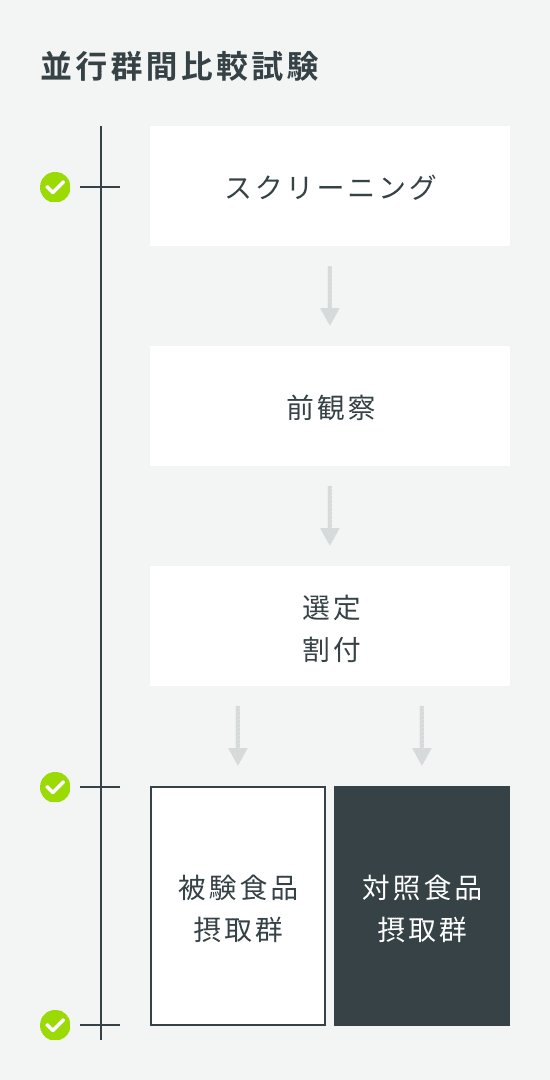
| 試験デザイン | クロスオーバー比較試験または並行群間比較試験 |
| 介入期間 | 2週間-12週間 |
| 検査回数 | クロスオーバー比較試験 5回:スクリーニング、第1期摂取開始前、第1期摂取終了時、第2期摂取開始前、第2期摂取終了時 並行群間比較試験 3回:スクリーニング、0W、2W |
| 症例数 | クロスオーバー比較試験 30名 並行群間比較試験 60名(1群30名×2群) |
| 対象 | PSQIスコアが6以上 |
| 評価項目 | 【機器測定】 スリープスコープ等の簡易脳波計での脳波計測定、眠りスキャン等の敷き型睡眠状況測定機器での睡眠時の活動測定、活動量計での睡眠時の活動測定 【アンケート】 ピッツバーグ睡眠調査票(PSQI)、起床時睡眠感調査票(OSA-MA)、エプワース眠気尺度(ESS)、アテネ式不眠尺度(AIS)、朝型-夜型質問票、自己評価版(MEQ-SA)、睡眠VAS |
アウトライン
運動機能試験
試験概要
| 研究目的 | 試験食品摂取による運動機能改善効果確認 |
|---|---|
| 説明 | 近年、アスリートや運動実施者のスポーツ栄養への注目が高まっています。 食品成分による筋肉量増加、筋力増強効果、また、運動後の過度な疲労や筋肉痛の軽減などについて多くの研究が行われています。またスポーツ栄養の研究成果は、老化予防の観点から、高齢者の栄養管理への応用が期待されています。 |
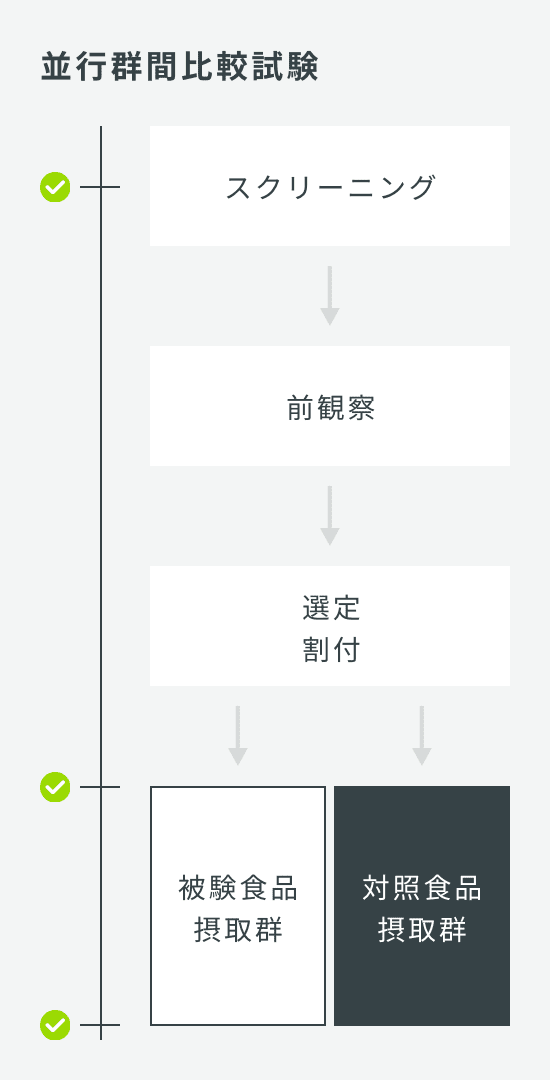
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 6回:スクリーニング1、スクリーニング2、0W、4W、8W、12W |
| 症例数 | 60名(1群30名×2群) |
| 対象 | 健常者 |
| 評価項目 | 【機器測定】 VO2MAXの変化、HRMAX75%テスト(エアロバイクのトレーニングテスト)検査機器ページ、無酸素パワーテスト、ウィンゲートテスト、(パワーマックスでのトレーニングテスト)検査機器ページ、握力、脚力 【アンケート】 VAS、ボルグスケール |
アウトライン
血糖値試験
試験概要
| 研究目的 | 試験食品摂取による血糖値の上昇抑制効果確認 |
|---|---|
| 説明 | 糖尿病は発症すると治癒することはなく、放置すると網膜症・腎症・神経障害等の合併症を引き起こし、末期には失明や、透析治療が必要となり、脳卒中、虚血性心疾患等の心血管疾患の発症・進展を促進することもあります。 血糖値を適正にコントロールすることは、糖尿病の発症予防において有効であると考えられています。 |
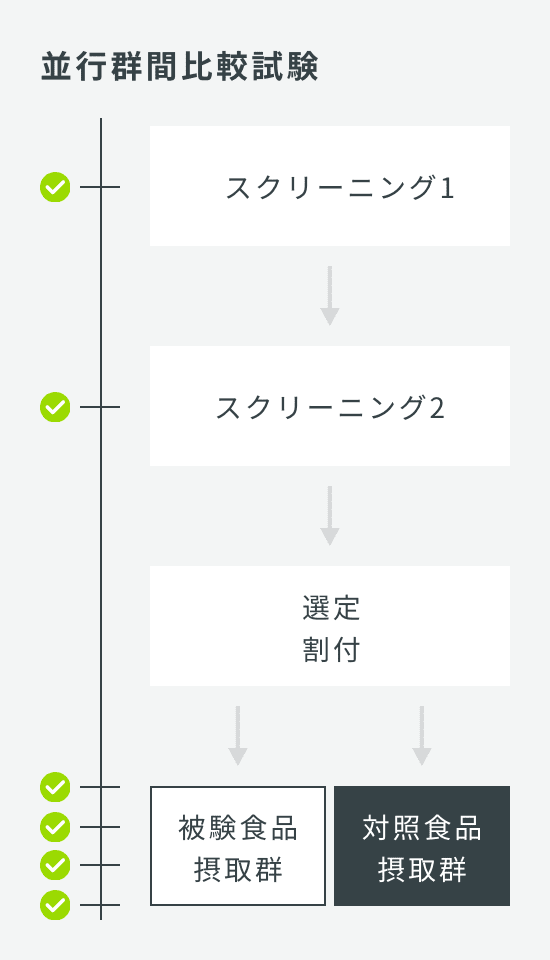
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回摂取 |
| 検査回数 | 3回:スクリーニング、第1期検査、第2期検査 |
| 症例数 | 30名 |
| 対象 | 空腹時血糖値が126mg/dL未満 |
| 評価項目 | 血糖、インスリン |
アウトライン
中性脂肪試験
試験概要
| 研究目的 | 試験食品摂取による血中中性脂肪値の上昇抑制効果確認 |
|---|---|
| 説明 | 中性脂肪は人間にとって重要なエネルギー源であり、必須脂肪酸の摂取にも関わっていますが、食事などから取り過ぎると体脂肪として蓄えられ、肥満や生活習慣病の原因となる恐れがあります。血液中の中性脂肪濃度を適切に保つことは、肥満や生活習慣病の予防に重要になります。 |
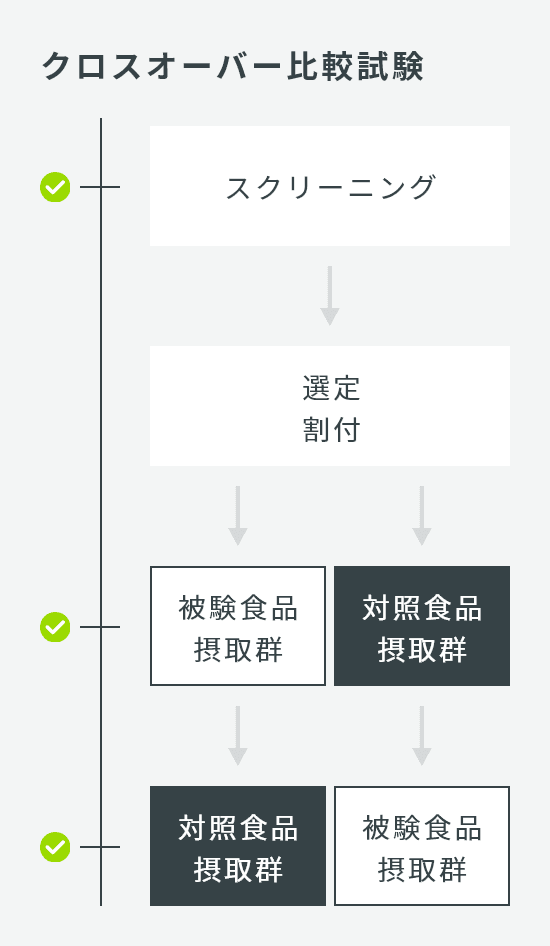
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回摂取 |
| 検査回数 | 3回:スクリーニング、第1期検査、第2期検査 |
| 症例数 | 30名 |
| 対象 | 空腹時の血中中性脂肪値が120以上200mg/dL未満 |
| 評価項目 | 中性脂肪値(検査機器ページ:デュアルスキャン) |
アウトライン
内臓脂肪試験
試験概要
| 研究目的 | 試験食品摂取による内臓脂肪低減効果確認 |
|---|---|
| 説明 | 心臓・脳血管疾患は、高血糖、脂質異常、高血圧などに起因する動脈硬化が進行することで発症しますが、主な原因は内臓脂肪の過剰蓄積を病態の中心とするメタボリックシンドロームと考えられています。 内臓脂肪を減らすことができれば、メタボリックシンドロームや生活習慣病及び心臓・脳血管疾患の発症を減らすことができると考えられています。 |
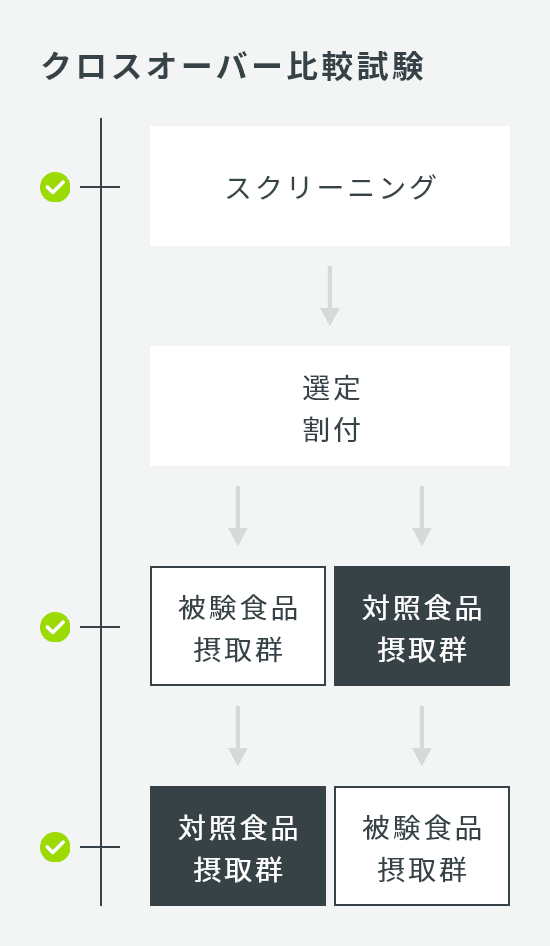
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 5回:スクリーニング、0W、4W、8W、12W |
| 症例数 | 100名(1群50名×2群) |
| 対象 | 健常者 |
| 評価項目 | 【機器測定】 腹部内臓脂肪面積(X線CT)、またはインピーダンス法による腹部内臓脂肪面積(デュアルスキャン)検査機器ページ、体重、体脂肪量 【血液検査】 総コレステロール、中性脂肪、HDLコレステロール、LDLコレステロール |
アウトライン
肌試験
試験概要
| 研究目的 | 試験食品摂取または試験品使用による肌質改善効果確認 |
|---|---|
| 説明 | 機能性食品や化粧品の素材を用いて、肌質を確認する試験を実施することができます。角層水分量(うるおい)や肌粘弾性(ハリ)などが評価できます。 |
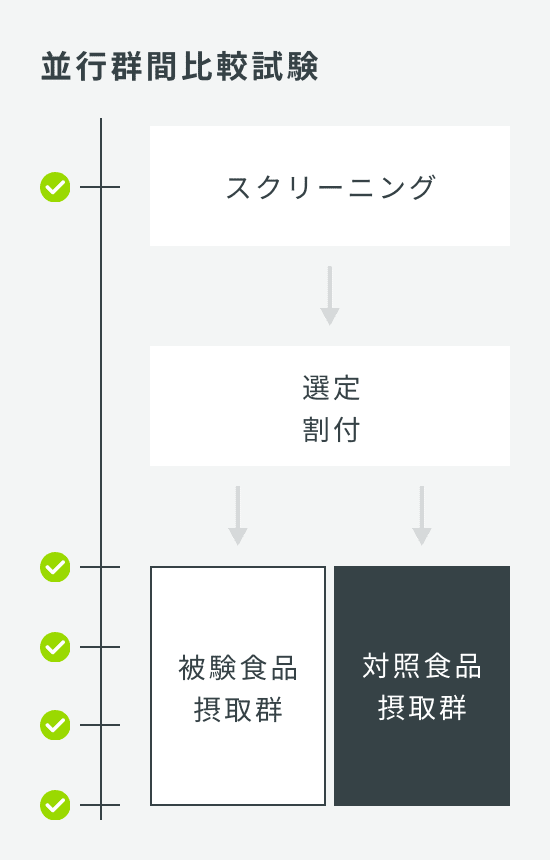
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 8週間 |
| 検査回数 | 4回:スクリーニング、0W、4W、8W |
| 症例数 | 40名(1群20名×2群) |
| 対象 | 肌の乾燥が気になる者 |
| 評価項目 | 【機器測定】 角層水分量、肌粘弾性、水分蒸散量、肌紅斑、肌油分 【画像解析】 VISIA撮影、肌色差検査機器ページ 【アンケート】 主観アンケート |
アウトライン
過剰摂取安全性試験
試験概要
| 研究目的 | 試験食品の過剰摂取による安全性確認 |
|---|---|
| 説明 | 試験食品を過剰摂取することによる安全性を確認します。 |
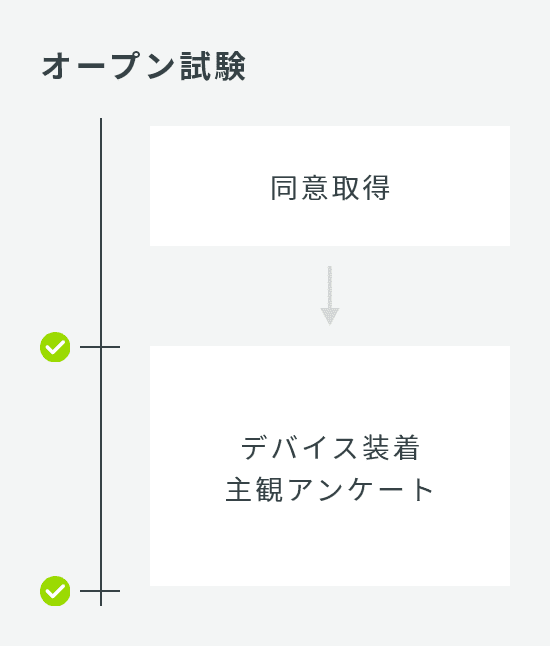
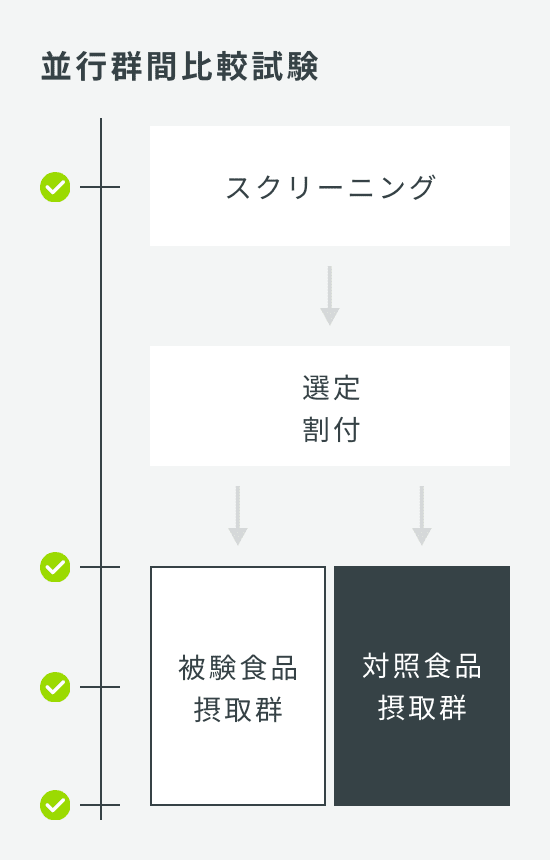
| 試験デザイン | オープン試験、または並行群間比較試験 |
| 介入期間 | 4週間 |
| 検査回数 | 5回:スクリーニング、0W、2W、4W、後観察2W |
| 症例数 | オープン試験 20名 並行群間比較試験 40名(1群20名×2群) |
| 対象 | 健常者 |
| 評価項目 | 血液学検査、血液生化学検査、尿一般検査、日誌による体調確認 |
アウトライン
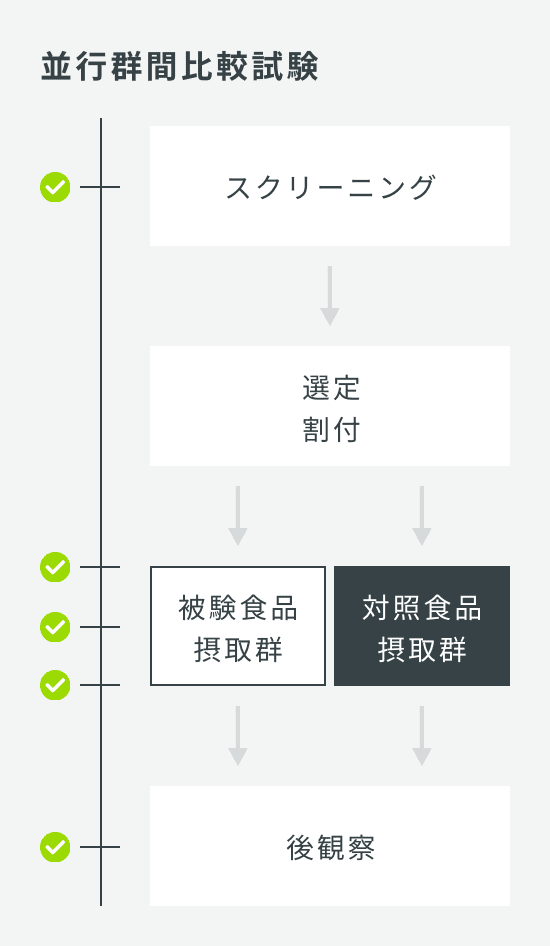
長期摂取安全性試験
試験概要
| 研究目的 | 試験食品の長期摂取による安全性確認 |
|---|---|
| 説明 | 試験食品を長期間摂取することによる安全性を確認します |
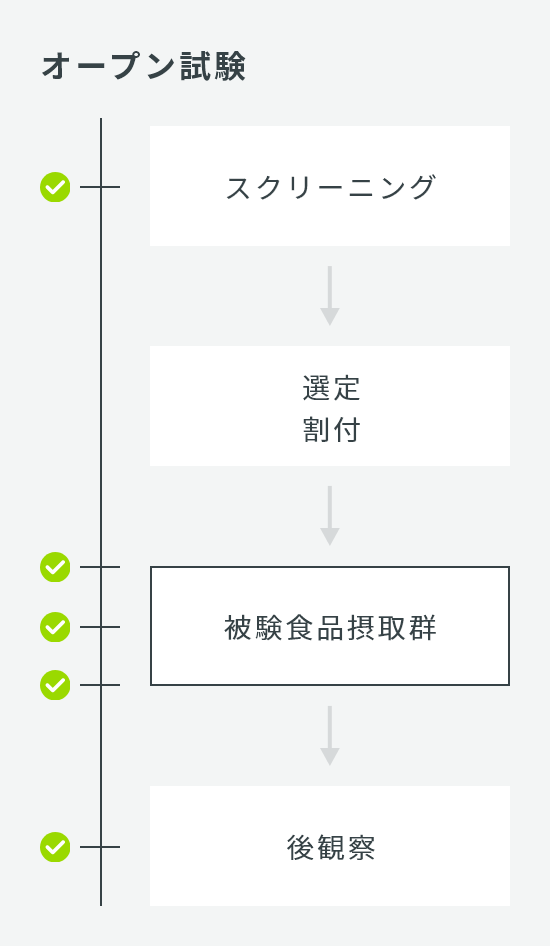
| 試験デザイン | オープン試験、または並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 6回:スクリーニング、0W、4W、8W、12W、後観察4W |
| 症例数 | オープン試験 20名 |
| 対象 | 健常者 |
| 評価項目 | 血液学検査、血液生化学検査、尿一般検査、日誌による体調確認 |
アウトライン
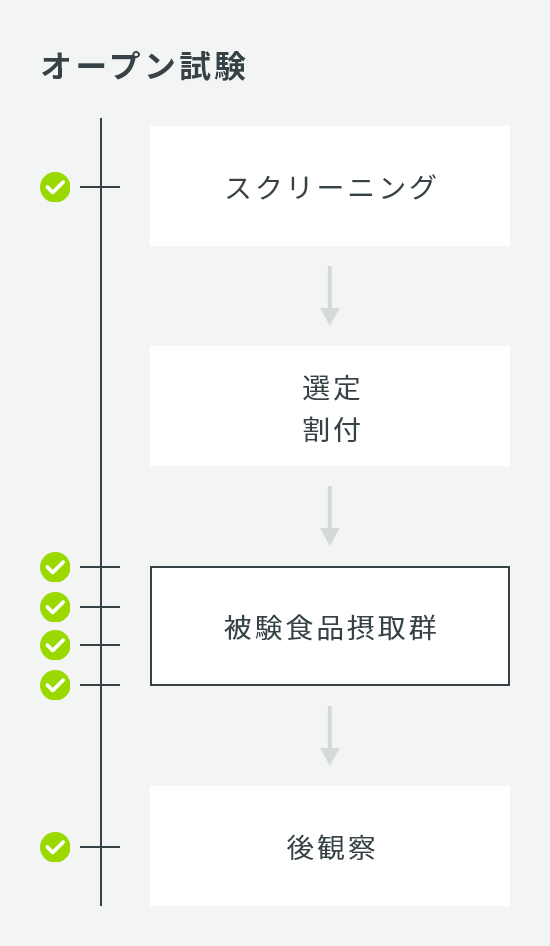
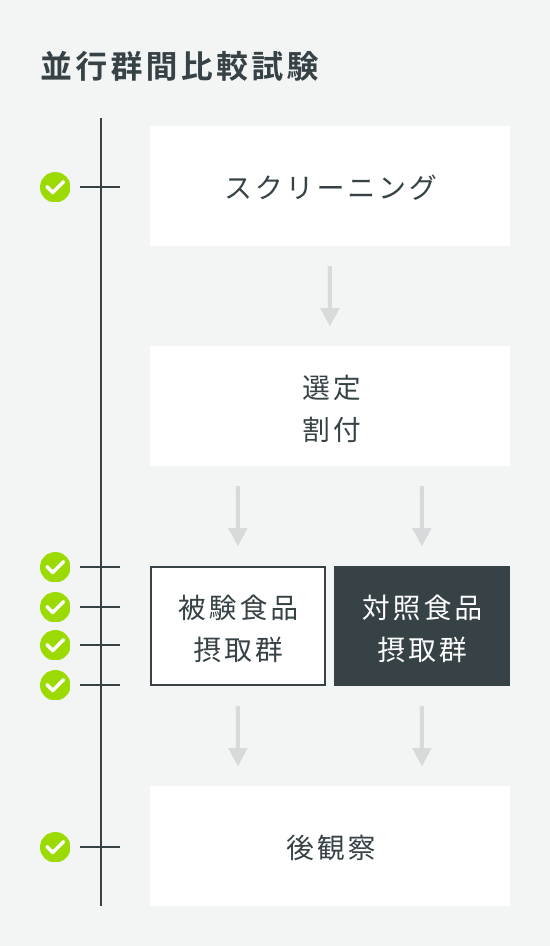
用量設定試験
試験概要
| 研究目的 | |
|---|---|
| 説明 | |
| 試験デザイン | |
| 介入期間 | |
| 検査回数 | |
| 症例数 | |
| 対象 | |
| 評価項目 |
アウトライン

過剰摂取安全性確認試験
試験概要
| 研究目的 | 試験食品の過剰摂取による安全性確認 |
|---|---|
| 説明 | 試験食品を過剰摂取することによる安全性を確認します。 |
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 4週間 |
| 検査回数 | 5回:スクリーニング、0W、2W、4W、後観察2W |
| 症例数 | 並行群間比較試験 40名(1群20名×2群) |
| 対象 | 健常者 |
| 評価項目 | 血液学検査 血液生化学検査 尿一般検査 日誌による体調確認 |
アウトライン

有効性確認試験(例:内臓脂肪試験)
試験概要
| 研究目的 | 試験食品摂取による内臓脂肪低減効果確認 |
|---|---|
| 説明 | 心臓・脳血管疾患は、高血糖、脂質異常、高血圧などに起因する動脈硬化が進行することで発症しますが、主な原因は内臓脂肪の過剰蓄積を病態の中心とするメタボリックシンドロームと考えられています。 内臓脂肪を減らすことができれば、メタボリックシンドロームや生活習慣病及び心臓・脳血管疾患の発症を減らすことができると考えられています。 |
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 5回:スクリーニング、0W、4W、8W、12W |
| 症例数 | 100名(1群50名×2群) |
| 対象 | 健常者 |
| 評価項目 | 【機器測定】 腹部内臓脂肪面積(X線CT)、またはインピーダンス法による腹部内臓脂肪面積(デュアルスキャン)、体重、体脂肪量 【血液検査】 総コレステロール、中性脂肪、HDLコレステロール、LDLコレステロール |
アウトライン

長期摂取安全性確認試験
試験概要
| 研究目的 | 試験食品の長期摂取による安全性確認 |
|---|---|
| 説明 | 試験食品を長期間摂取することによる安全性を確認します |
| 試験デザイン | 並行群間比較試験 |
| 介入期間 | 12週間 |
| 検査回数 | 6回:スクリーニング、0W、4W、8W、12W、後観察4W |
| 症例数 | 並行群間比較試験 40名(1群20名×2群) |
| 対象 | 健常者 |
| 評価項目 | 血液学検査 血液生化学検査 尿一般検査 日誌による体調確認 |
アウトライン

便通パイロット
試験概要
| 研究目的 | 試験食品摂取による便通改善効果の探索的確認 |
|---|---|
| 説明 | 便秘による体の不調は腹痛、腹部膨満感、食欲不振、肌荒れや肩こりなど、全身に影響が出ることもあります。便秘を改善することは各種疾病予防へ繋がり、生活の質を高めることができます。 |
| 試験デザイン | オープン試験 |
| 介入期間 | 4週間 |
| 検査回数 | 3回:スクリーニング、0W、4W |
| 症例数 | 15名 |
| 対象 | 便秘傾向者 |
| 評価項目 | 日誌での排便回数やブリストルスケール CAS-MT |
アウトライン
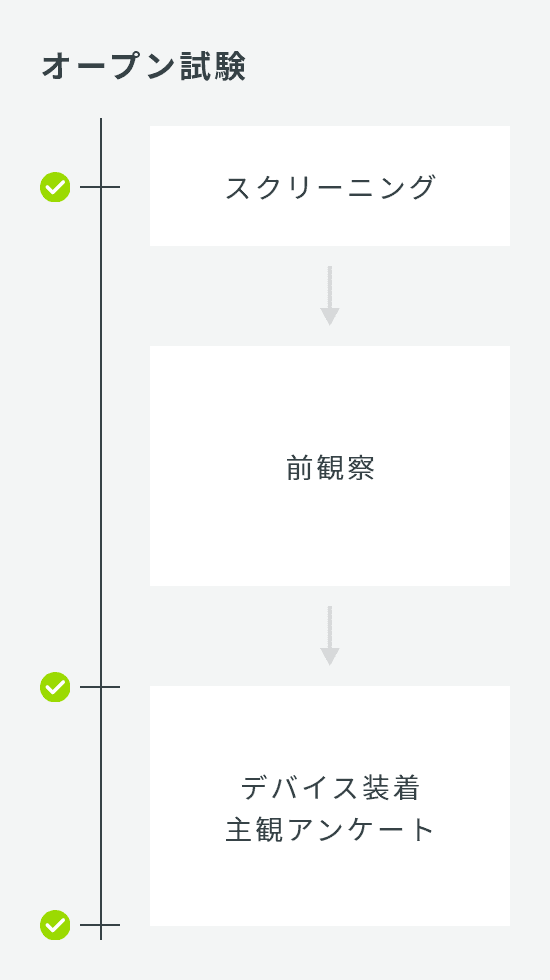
肌パイロット
試験概要
| 研究目的 | 試験食品摂取または試験品使用による肌質改善効果確認 |
|---|---|
| 説明 | 機能性食品や化粧品の素材を用いた試験を実施することができます。 |
| 試験デザイン | オープン試験 |
| 介入期間 | 4週間 |
| 検査回数 | 2回:スクリーニング兼摂取(使用)前、4W |
| 症例数 | 15名 |
| 対象 | 肌の乾燥が気になる者 |
| 評価項目 | 角層水分量 肌粘弾性 水分蒸散量 主観アンケート |
アウトライン
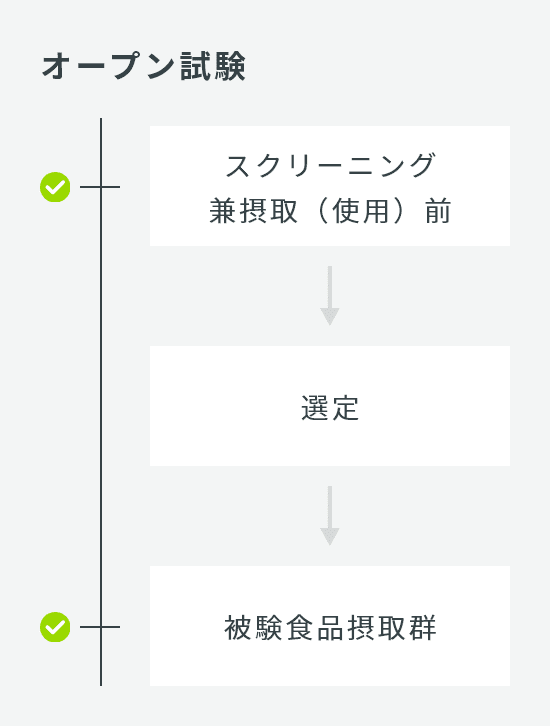
唾液分泌促進パイロット
試験概要
| 研究目的 | 試験食品摂取による唾液分泌機能改善効果確認 |
|---|---|
| 説明 | 加齢やストレスにより口腔内が乾いたり唾液量が少なくなると、口腔内に細菌が繁殖しやすくなり、口臭の原因になります。また、口腔機能が低下することにより、様々な病気を引き起こす原因にもなります。 |
| 試験デザイン | クロスオーバー比較試験 |
| 介入期間 | 単回摂取、2期 |
| 検査回数 | 3回:スクリーニング、第1期、第2期 |
| 症例数 | 15名 |
| 対象 | 口腔が乾きやすい自覚がある健常者 |
| 評価項目 | 刺激時唾液量測定(試験食品の摂取前、摂取○分後、摂取○分後) |
アウトライン
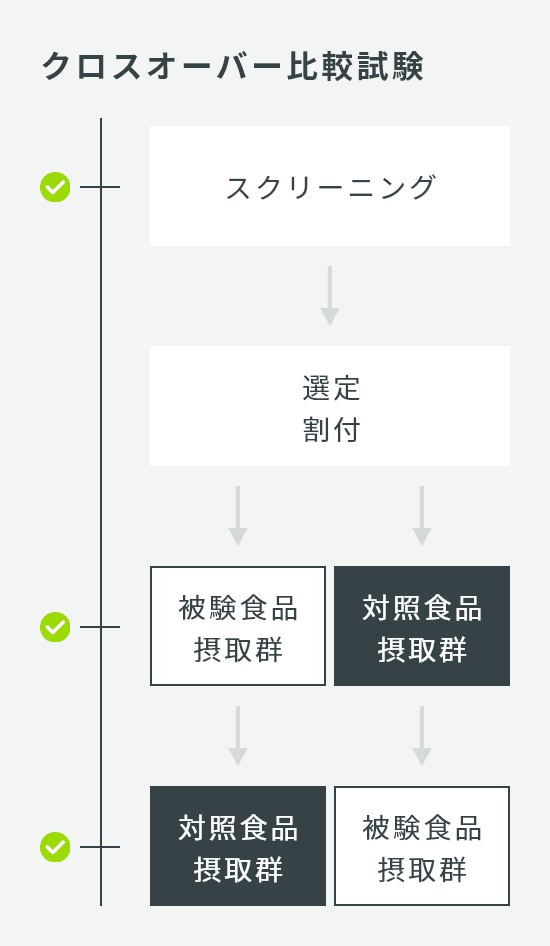
試験品嗜好性調査
試験概要
| 研究目的 | 試験品使用による嗜好性調査 |
|---|---|
| 説明 | 試験品の味、香り、食感、飲みやすさ、食べやすさなどの嗜好性を確認することでマーケティング調査を行うことができます。 |
| 試験デザイン | オープン試験 |
| 介入期間 | 1日または複数日 |
| 検査回数 | 1回または複数回 |
| 症例数 | 100名~ |
| 対象 | 健常者 |
| 評価項目 | 嗜好性アンケート フリーアンサー |
アウトライン
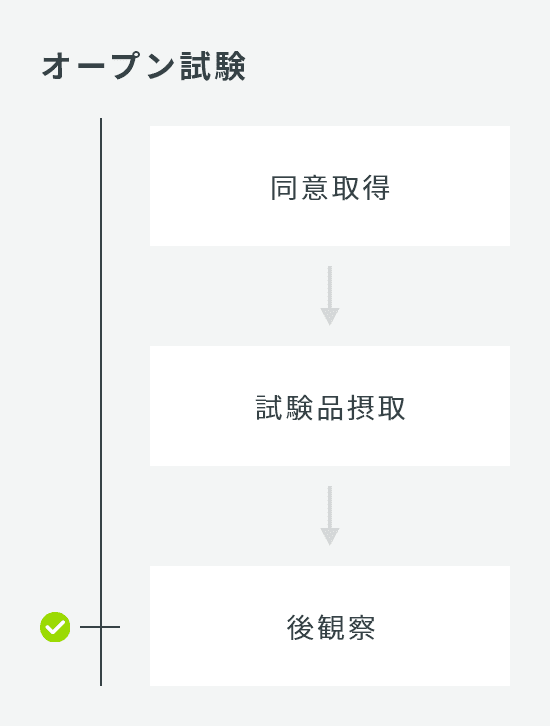
デバイス使用感調査
試験概要
| 研究目的 | デバイスを使用することによる各種調査 |
|---|---|
| 説明 | デバイスを使用することによる各種の調査を行うことで販売促進、マーケティングデータの取得が可能です。 |
| 試験デザイン | オープン試験 |
| 介入期間 | 1週間~4週間 |
| 検査回数 | 2回(開始時、終了時) |
| 症例数 | 100名~ |
| 対象 | 健常者 |
| 評価項目 | デバイスで取得可能なデータ 主観アンケート |
アウトライン